Сертификация импортных лекарственных препаратов в КНР
Содержание:
1.Порядок регистрации лекарственного препарата в КНР
2.Документы, прилагаемые к заявлению для импортных препаратов
3.Правила GCP
Порядок регистрации лекарственного препарата в КНР
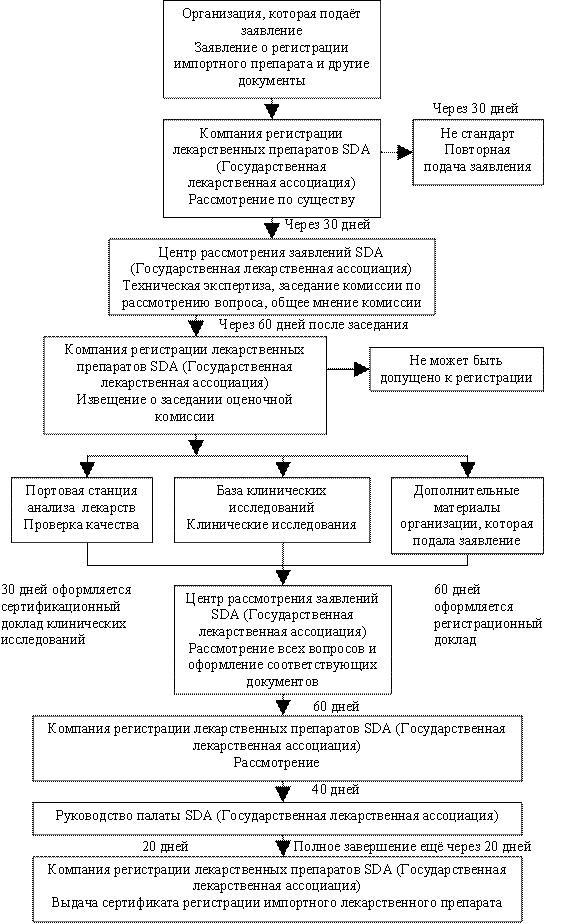
Для прошения о регистрации импортного лекарственного препарата необходимо представить нижеследующие материалы:
- Сертификат и нотариальное свидетельство государственной компетентной организации лекарственной сферы в стране производства препарата удостоверяющие, что препарат зарегистрирован, производится, продаётся и экспортируется, а завод-производитель работает в соответствии с нормативами производства лекарств GMP. (Все документы в подлиннике по форме WHO, если нужно, они заверяются в консульстве нотариусом).
- Доверенность китайского посредника в том, что зарубежный производитель и продавец лекарства уполномочил его подать заявление от своего лица.
- Копия свидетельства на право производственной и коммерческой деятельности китайского посредника.
- Копия свидетельства о регистрации китайского постоянного представительства зарубежного завода-производителя и продавца лекарств.
- (Если нет представительства, то через китайского посредника, если есть представительство, то самостоятельно, с копией свидетельства об открытии представительства).
- Патентное свидетельство для лекарственного препарата.
- Инструкция по применению лекарства, заверенная государственной компетентной организацией лекарственной сферы в стране производства препарата.
- Стандарт качества препарата и способы проверки.
- Записи результатов объектных исследований препарата.
- Рецептура препарата, технология производства, фармакология, токсикология, а также клинические исследования и другая подробная техническая документация.
- Образцы препарата, упаковки и другие материалы.
Конкретные требования к заявляемым материалам соответствуют прилагаемым к данным правилам “Подробным нормам об импортных лекарственных препаратах”
- При проведении клинических испытаний исследователи всего мира руководствуются основными правилами GCP (качественной клинической практики).
- Организационными нормами клинических опытов для лекарств GSP
- Правилами доклинических исследований лекарственных средств (GLP),
- Правилами клинических исследований (GСP),
- Правилами организации производства и контроля качества лекарственных средств (GMP),
- Правилами оптовой торговли лекарственными средствами (GDP, GSP)
- и Правилами розничной торговли лекарственными средствами (GPP).